最初に変性疾患の診断を下した医者が、その患者さんを最後までフォローすることは、恐らくだが殆どないと思われる。
施設入所などをきっかけに主治医が変更になると、病名と薬は概ね引き継がれる。
しかし、最初に診断した医者だけが持ち得た診断に当たっての根拠や確信、そして「ひょっとしたら別の変性疾患かも・・・」といった違和感まで引き継がれることはない。
70代女性 DLB→PSP→CBD?
3年前に、B病院でレビー小体型認知症(DLB)と診断されたOKさん。
その後、C病院で進行性核上性麻痺(PSP)に診断が変更となった。現在は施設に入居し、施設嘱託医がかかりつけ医として、前医の処方をそのまま引き継いでいた。
ご家族に伴われて車椅子で来院されたOKさんの、左前に大きく前傾した姿勢と左上下肢を動かしにくそうにしている様子をみて、自分は「大脳皮質基底核変性症(CBD)の可能性は?」と考えた。
内服を確認したところ、
- アリセプト5mg 朝食後
- メネシット600mg分3 毎食後
- ゾニサミド25mg 朝食後
- テトラミド10mg 眠前
この4種類。ご家族に聞くと、長らくこの内容で変化はないとのことであった。
アリセプト5mgは、診断がDLBだった頃の名残なのだろうか。メネシット600mgは、PD(パーキンソン病)ではない方にはちょっと多すぎる印象。またゾニサミドだが、恐ろしく値段の高いトレリーフを使っていないだけ良心的とは言えるが、これもやはり診断がDLBの頃の名残と思われた。
眠前テトラミドについては、精神科では眠剤代わりに使われているのを時に目にする。善し悪しは不明だったが、聞けば今のところ、睡眠に関しては困ってはいないようだった。
MIBG心筋シンチの結果が優先され、DLBの診断
OKさんはまず、物忘れや計算が苦手になるなどの認知機能低下が先行し、その後歩行や発語が緩慢になってきた頃にB病院を受診した。
MRI、SPECT、DATスキャン、MIBG心筋シンチという"フルコース"精査の結果、「誘因のないパーキンソニズム(中核的症状)+DATスキャンによる取り込み低下(支持的特徴)」という結果から、DLBの診断がおりた。

早期、後期、いずれも取り込み低下
これは、B病院から取り寄せたOKさんのMIBG心筋シンチの結果だが、早期と後期、いずれも著明な取り込み低下を示している。
心不全や糖尿病のない方なので、これはPDまたはDLBの可能性を強く示唆する所見である。*1
MIBG心筋シンチは、パーキンソン病(PD)と他のパーキンソニズムを呈する疾患を鑑別するのに有用とされる検査である。
多系統萎縮症(MSA)やPSP、CBDなどと、PDを鑑別する際の感度と特異度は後期像ではそれぞれ89.7%と82.6%と報告されている。*2
DLBの診断基準(2017年)においては、これまでの「支持的バイオマーカー」から「指標的バイオマーカー」に格上げされたということがあり、今後これまで以上にMIBG心筋シンチは診断に活用されていくと思われる。
ところで、先述した「誘因のないパーキンソニズム(中核的特徴)+DATスキャンで取り込み低下(支持的特徴)」というAさんの診断根拠だが、これは2005年の診断基準に基づいたものである。
2017年の診断基準(認知症疾患診療ガイドライン2017より引用)では、中核的特徴は
- 注意や明晰さの著明な変化を伴う認知の変動
- 繰り返し出現する構築された具体的な幻視
- 特発性パーキンソニズムの以下の症状のうち1つ以上:動作緩慢、寡動、静止時振戦、筋強剛
- 認知機能の低下に先行することもあるレム睡眠行動異常
の4つとなっている*3。2005年Ver.に、4の「レム睡眠行動異常」が加わったことが大きな変化である。
そして、Probable DLB(ほぼ確実にDLB)と診断するには、
- a. 2つ以上の中核的臨床的特徴が存在する
- b. 1つの中核的臨床的特徴が存在し、1つ以上の示唆的バイオマーカーが存在する
aまたはbを満たすことが必要、となっている。
OKさんは、bに当てはまる。即ち、「中核的特徴の3」+「MIG心筋シンチで取り込み低下+DATスキャンで取り込み低下」である。2005年、2017年の診断基準、いずれにも該当するということである。
ただ、個人的な感想としては、複数のバイオマーカーによる支持があっても、認知の変動や幻視、レム睡眠行動異常、いずれも伴わない方をDLBとは診断し難いように思う。
DLBと診断する根拠となる中核的特徴がパーキンソニズムだけという方は、自分の経験を遡ってもちょっと思い出せない。
最初からPSPであった可能性は?
DLBと診断された約2年後に、OKさんはC病院でPSPと診断された。
C病院からは資料の取り寄せが出来ず、その診断根拠や検査結果について詳細はわからなかった。
PSPの診断根拠として有名な「垂直方向への眼球運動障害」については、確認が困難であった。
それは、頚部の前屈と体幹の前方への倒れ込みが強かったからである。何とか下に潜り込むような格好で確認を試みたが、軽度眼位の異常を感じはしたものの、眼球運動については正直よく分からなかった。
すくみ足と寡動、無言は印象的だったので、PSPであればPSP-PAGFなのかな?とは思った。
DLBと診断したB病院から提供して頂いたMRI画像を以下に示す。
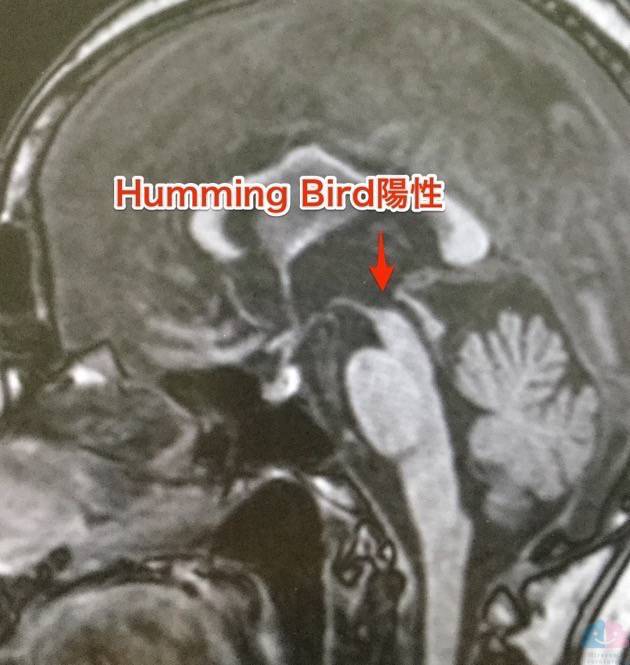
Humming Birdサイン陽性
PSPの画像的特徴とされることの多いHumming Birdサインは陽性であった。
因みに、Humming BirdサインはPSPと診断するための必要条件ではない。
中脳被蓋の面積を測定してみると、
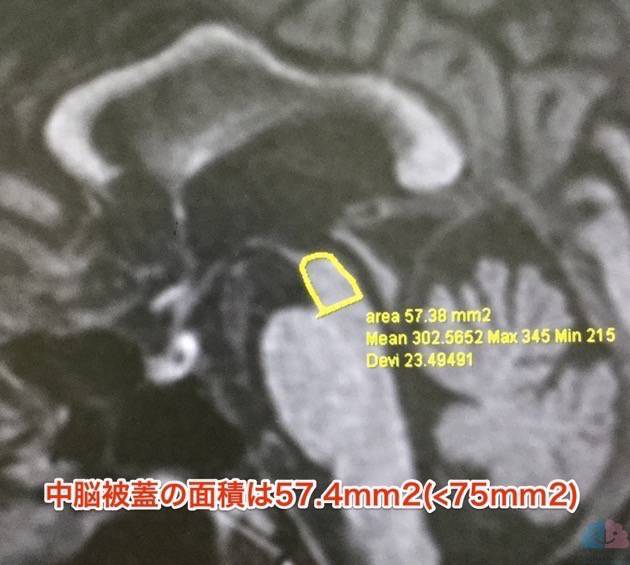
中脳被蓋の面積は57.4mm
57.4mm2と、萎縮は明らかであった。*4
変性疾患の診断は、途中で変わりうる
PSPやCBD、MSAなどのいわゆる"パーキンソン関連疾患"とDLBは、特に病初期においては区別が難しいことが多々あるため、MIBG心筋シンチやDATスキャンなどの結果をバイオマーカーとして利用することに、一定の意義はある。
ただ、以下のような剖検例の存在は、バイオマーカーに頼りすぎることの危うさを教えてくれるように思う。
症例は死亡時 86 歳の男性である.進行性の歩行障害,筋強剛,認知症を呈した.静止時振戦,L-dopa の反応性,自律神経障害はなかったが,MIBG 心筋シンチグラフィーの集積低下をみとめ,Lewy 小体型認知症と臨 床診断された.死亡後の病理診断は大脳皮質基底核変性症であった.全身病理では心臓交感神経終末が高度に脱落 しており,MIBG の集積低下を反映していた.さらに中枢神経,消化管,副腎等にはみられなかった Lewy 小体が交 感神経節に限局してみとめられた.MIBGの集積低下はLewy小体の存在を示唆するが,その広がりまでは予見できず,また偶発的にLewy小体が合併する事を臨床診断の際には考慮する必要がある.(臨床神経 2012;52:405-410) ※赤文字強調は筆者によるもの
結局、OKさんが現時点でPSPなのかCBDなのか、確たる判断はつかなかった。
DLBの可能性については上記したように、最初のMIBG心筋シンチの結果を踏まえた上でも相当低いとは思った。
B病院のMRIやSPECTでは明らかな萎縮の左右差はなく、「CBDを示唆するかな?」と感じた前傾姿勢や左上下肢運動の拙劣さも、有意な所見とまでは言い難かった。
ただ、いずれにしても冒頭で示した処方内容は不適切と思われたので、かかりつけ医に減量するように依頼して、グルタチオン点滴療法を開始した。
点滴回数は合計19回。
使用したグルタチオンの一回当たりの量は、1800~3000mg。ビタミンB1やB2、B12、その他シチコリンやノイロトロピンなどを、用量を工夫しながら併用した。
経過中に、活気上昇や介助量減少が得られた時期はあった。これは、グルタチオン点滴の効果以外に内服薬の減量効果もあったと思っている。*5
点滴の間隔が10日以上空くと動きが悪化するとのことで、7日間隔でご家族が連れて来られた時期もあった。
およそ7ヶ月の試行錯誤の末、徐々に運動面低下をきたしていったAさん。
ご家族が連れて来られるご負担も考慮した上で、点滴によるサポートは一旦終了となった。
またお会い出来る日があれば、今度は処方も一切合切ひっくるめてお付き合い出来たらと思っている。